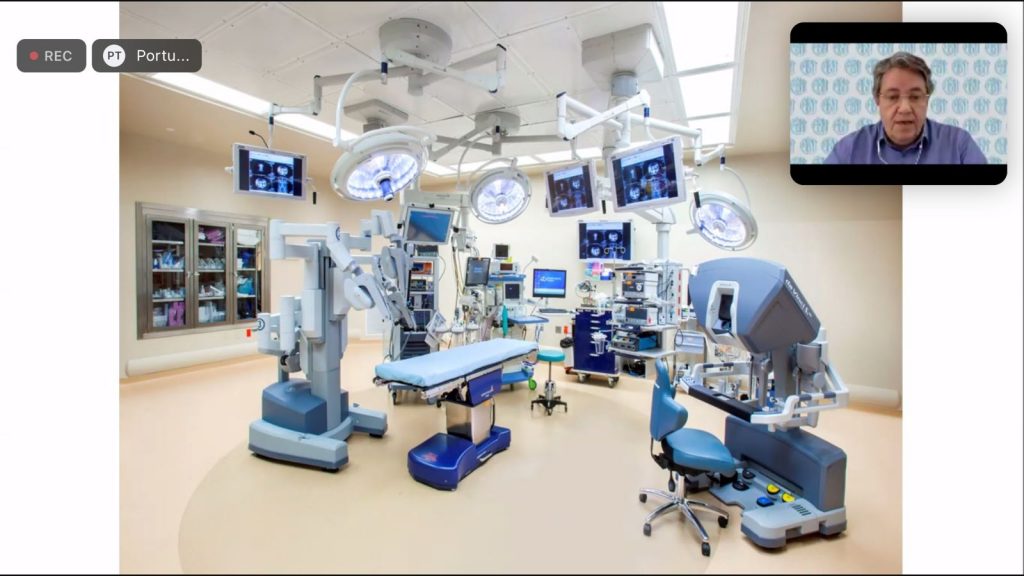
Seminário Internacional sobre Dispositivos Médicos teve mais de 600 participantes, lideranças do setor de saúde de onze países, com transmissão simultânea em inglês e espanhol
O Brasil tem, atualmente, cerca de 80 mil dispositivos médicos (DMs) registrados pela Agência Nacional de Vigilância Sanitária. São produtos que acompanham o paciente do nascimento ao fim da vida e que, na pandemia da Covid-19, ganharam protagonismo. “Esse setor tem que ser estratégico na agenda de desenvolvimento brasileira”, afirmou o presidente da Aliança Brasileira da Indústria Inovadora em Saúde, Bruno Boldrin Bezerra, na abertura do Seminário Internacional ‘Dispositivos médicos: regulação, avanços e perspectivas’, realizado nos dias 22 e 23 de novembro, com o apoio da Anvisa, da Coalizão Interamericana de Convergência Regulatória no setor de Dispositivos Médicos (IACRC) e da United States Agency For International Development (USAID). Participaram mais de 600 lideranças do setor de saúde do Brasil, Canadá, Colômbia, Coreia do Sul, Espanha, Estados Unidos, México, Moçambique, Paraguai, Peru e Suíça.
O evento marcou os 10 anos da Aliança, que trabalha para aprimorar a inovação em saúde no país. “A ABIIS e parceiros têm atuado para que possamos avançar ainda mais em boas práticas regulatórias. Todos os mecanismos de regulação inteligente que defendemos são para permitir o maior acesso do paciente às tecnologias e também um desenvolvimento de todo o setor, não só no Brasil, mas também nas Américas”, disse Bezerra. O executivo destacou ainda a aprovação pelo Congresso Nacional, em tempo recorde, do Protocolo ao Acordo de Comércio e Cooperação Econômica entre o Brasil e os Estados Unidos. “A Aliança, em parceria com a Confederação Nacional da Indústria e a Amcham, trabalhou intensamente, desde a assinatura no ano passado e durante a tramitação no Legislativo, para demonstrar a importância desse Acordo para toda a economia brasileira, em especial para o setor saúde”.
‘O contexto das Boas Práticas Regulatórias e a Convergência Regulatória para Dispositivos Médicos nas Américas’ foi tema do primeiro painel, com a participação de Leticia Fonseca, da IACRC. Em seguida, Cristiane Rose Jourdan Gomes, da Anvisa apresentou o ‘novo processo regulatório da Anvisa para implementação das Boas Práticas Regulatórias’. Atualmente, a Agência Nacional de Vigilância Sanitária tem 146 projetos regulatórios prioritários. Rodrigo Taveira, da Gerência-Geral de Regulamentação e Boas Práticas Regulatórias (GGREG) apresentou o ciclo regulatório e revelou que do ano passado para cá, mais de 1200 normas foram avaliadas, mais de 800 normas revogadas e 110 normas consolidadas. Debora Ferreira, da Boston Scientific, também esteve no debate que foi moderado pelo diretor executivo da ABIIS, José Márcio Cerqueira Gomes.
O vice-presidente da Advanced Medical Technology Association (Advamed), Steven Bipes, deu início ao debate sobre ‘Uso de normas internacionais para tecnologia médica para convergência regulatória no Brasil e no mundo’ destacando a política coerente de boas práticas no Brasil, considerando o uso de padrões internacionais para fins normativos e regulatórios. Neste contexto, os Comitês Brasileiros de Odonto-Médico Hospitalar e de Análises Clínicas e Diagnóstico in Vitro da Associação Brasileira de Normas Técnicas têm papel importantíssimo. E a participação de cada stakeholder do setor privado e do governo na elaboração dessas normas internacionais ajuda bastante nesse esforço para convergência regulatória”, disse. Joffre Moraes e Humberto Tibúrcio apresentaram as normas referentes aos dois comitês da ABNT.
A avaliação de conformidades foi tema do último painel do primeiro dia de evento, com a participação de Danilo Marques, daSmith Nephew, Anderson Pereira, da Anvisa, Davison Silva, da Agência Nacional de Telecomunicações (Anatel), e Lenilton Duran Pinto Correa, do Instituto Nacional de Metrologia, Qualidade e Tecnologia (Inmetro).
O evento completo e todas as apresentações dos palestrantes em PDF estão disponíveis clicando aqui.