Objetivo é divulgar resultados das análises dos itens avaliados.
No enfrentamento à pandemia de Covid-19, dar transparência aos dados sobre produtos sujeitos à vigilância é uma das ações estratégicas adotadas pela Anvisa, que conta com painéis abertos ao público para consulta de informações. Por meio de plataformas de Business Intelligence (BI), são divulgados os resultados do monitoramento desses produtos e de testes de diagnóstico para Covid-19.
Uma das plataformas é a de Monitoramento pós-mercado da qualidade de produtos sujeitos à vigilância sanitária – Covid-19, que traz dados sobre produtos que estão ou estiveram em situação de irregularidade.
Neste trabalho, alguns dos resultados que desencadeiam ações da Anvisa são o desempenho insatisfatório dos produtos testados, falta de Certificação de Boas Práticas de Fabricação (CBPF) ou de regularização de Autorização de Funcionamento (AE), ausência de registro, rotulagem irregular, entre outros motivos.
As informações sobre as ações de fiscalização estão no painel, distribuídas por categorias (produtos para saúde e diagnóstico in vitro, além de saneantes e cosméticos) e em quadro organizado pelo nome da empresa responsável, produtos, lotes inspecionados e ações realizadas.
A Anvisa esclarece que, caso a empresa apresente adequação às normas e uma solução para o problema detectado, as medidas podem ser revogadas. Por isso, o painel também tem informações sobre a situação do produto e um link da publicação da medida adotada.
De acordo com os dados disponíveis na plataforma até 26 de agosto, 102 medidas já haviam sido adotadas. Os dados analíticos mostram que a maior parte dos produtos alvo de medidas restritivas são cosméticos (43,27%), categoria na qual estão, por exemplo, produtos com álcool usados como antissépticos para mãos. Em seguida estão os saneantes (33,65%), produtos para diagnóstico in vitro (17,31%) e demais produtos para saúde (5,77%).
Testes para Covid-19
Há também a plataforma com dados do Monitoramento pós-mercado da qualidade de dispositivos para diagnóstico in vitro da Covid-19: análises laboratoriais, resultado de uma parceria entre a Anvisa e o Instituto Nacional de Controle de Qualidade em Saúde (INCQS), vinculado à Fundação Oswaldo Cruz (Fiocruz).
Nesta ação, o objetivo é aferir, por meio de ensaios laboratoriais, o desempenho e a precisão dos produtos colocados para consumo no país, visando garantir a segurança e a eficácia dos testes de diagnóstico.
As medidas indicadas após a avaliação do INCQS e da Anvisa podem ser de: interdição cautelar (ação preventiva); suspensão de fabricação, comercialização, distribuição, importação e uso; apreensão, inutilização e recolhimento. As medidas são publicadas pela Agência no Diário Oficial da União (D.O.U.).
O painel traz dados organizados sobre a quantidade de análises realizadas, resultados obtidos e medidas cautelares adotadas. Há também um quadro com o nome comercial do produto, a identificação do fabricante, o número do lote(s) analisado(s), do tipo do laudo e sua data da emissão. Tem ainda uma coluna com informações da análise realizada e outra com os links das resoluções com as medidas da Anvisa.
A Agência informa que, até o momento, foram publicadas interdições cautelares para os lotes de produtos reprovados em análises fiscais iniciais e foi feito o recolhimento de lotes de produtos reprovados também nas análises fiscais de contraprova.
Em se tratando de laudos de tipo controle, a Anvisa dá imediata publicidade aos resultados analíticos, garantindo o acesso à informação para a tomada de decisão pelos interessados, tais como o Ministério da Saúde, secretarias de Saúde, governos dos estados e municípios, hospitais, clínicas e a sociedade em geral. Adicionalmente, a Agência segue os ritos administrativos para coleta de amostras para realização das análises do tipo fiscal previstas na Lei 6.437/77.
Das 216 amostras analisadas até o dia 26/8, 134 produtos estão em conformidade com o desempenho esperado. Outros 82 não tiveram desempenho de acordo com o que foi alegado pelo fornecedor, sendo classificados como “não conformes”. Veja abaixo os resultados até o momento, por tipo de teste avaliado.
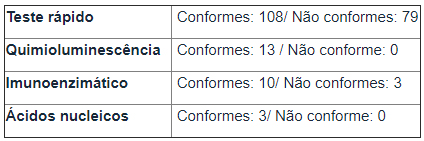
Rotineiramente, os dados analíticos obtidos no monitoramento de testes para diagnóstico e as medidas adotadas pela Anvisa são atualizados em um Painel Analítico público. Alista de produtos regularizados também é atualizada diariamente no portal da Agência.
É importante esclarecer que, de acordo com as regras atuais para concessão desses registros, não são realizados ensaios laboratoriais prévios pela Anvisa ou pelo INCQS. A responsabilidade pelas informações prestadas é do detentor do registro e o controle da produção deve seguir os preceitos das boas práticas de fabricação (BPF).
Notificação de eventos adversos
A Anvisa ressalta, ainda, que é essencial que os profissionais de saúde notifiquem ao órgão os eventuais problemas identificados durante o uso dos produtos para diagnóstico in vitro da Covid-19. Os dados das notificações são recebidos pela Agência e agrupados para fornecer subsídios necessários ao planejamento e à execução de ações de campo, fiscalização, inspeções e coletas de amostras para análises fiscais.
Com informações do site da ANVISA (01/09/2020)


