Documento esclarece dúvidas referentes ao carregamento de documentos sobre instruções de uso e rotulagem de produtos para saúde. Confira!
A Anvisa acaba de divulgar um documento orientativo sobre o protocolo de petições relacionadas àResolução da Diretoria Colegiada (RDC) 431/2020, que trata do carregamento de instruções de uso no portal eletrônico da Anvisa, vinculado aos processos de regularização de dispositivos médicos e dá outras providências.
Na publicação, a Gerência Geral de Tecnologia de Produtos para Saúde (GGTPS) esclarece as principais dúvidas sobre o tema. Além disso, apresenta o passo a passo para o protocolo de petição de Disponibilização de Instruções de Uso.
Vigente desde 1º de novembro, a norma informa que o carregamento se refere à inserção e à atualização das instruções de uso de dispositivos médicos em processo de regularização. Essas instruções correspondem a manuais e dados técnicos que orientam o comprador sobre as características do produto e trazem advertências, precauções e contraindicações relacionadas ao dispositivo, entre outras informações.
É importante esclarecer que o carregamento de instruções de uso é obrigatório e de responsabilidade do detentor da regularização do produto. Além disso, ele deverá ser controlado pela empresa para o caso de uma eventual auditoria da Agência. As informações devem estar de acordo com a legislação sanitária e corresponder ao produto regularizado.
As imagens do produto, bem como a sua rotulagem, podem ser carregadas voluntariamente e executadas diretamente pela empresa responsável pela notificação ou registro do produto. Destaca-se ainda que as instruções de uso carregadas constituem uma importante fonte de informação para pacientes, usuários, compradores, serviços de saúde, operadoras de planos de saúde, órgãos públicos licitantes, órgãos públicos de controle, serviços de auditoria, grupos de pesquisa em universidades, possibilitando inclusive a identificação de eventuais falsificações no mercado.
Prazos
Qualquer dispositivo médico regularizado após o dia 1º de novembro deste ano deve ter suas instruções de uso carregadas em até 30 dias, a contar da data de conclusão do parecer favorável da Anvisa para a regularização do produto. Esse prazo vale também para produtos regularizados já existentes e em comercialização que passem por alterações que modifiquem suas instruções de uso.
De modo a estabelecer um prazo exequível ao setor produtivo, do menor ao maior porte, o carregamento de instruções de uso para os demais dispositivos médicos regularizados (no passado) terá um período de transição de 12 meses, ou seja, as empresas terão esse prazo para terem suas instruções de uso carregadas, a contar do dia 1º de novembro.
No caso de o dispositivo médico regularizado não possuir as instruções em forma de manual ou material similar, a empresa deverá carregar no portal da Agência o modelo de rotulagem do produto no campo das instruções de uso. Ou seja, nesses casos valerá o conteúdo da embalagem.
Ressalta-se que o carregamento de instruções de uso será divulgado exclusivamente no portal da Anvisa, no momento da finalização do protocolo da petição. Havendo novo carregamento, serão mantidas públicas somente as últimas informações enviadas pela empresa. As instruções de uso carregadas ao longo do tempo serão mantidas em um banco de dados para controle e auditoria por parte da Agência.
Os documentos carregados podem ser acessados por meio da Consulta de Produtos Regularizados. Para realizar a busca, basta procurar pelo produto desejado e conferir os documentos disponíveis.
Abrangência
A Anvisa informa que a norma se aplica aos produtos regulados pelas RDCs 185/2001, 36/2015 e 40/2015 e atos normativos posteriores. Esclarece também que a RDC 431/2020complementa a Instrução Normativa (IN) 4/2012, que estabelece regras para instruções de uso de produtos para saúde em formato não impresso.
O descumprimento das regras poderá levar à suspensão da comercialização, importação e/ou uso do produto até o adequado carregamento das instruções no portal da Anvisa.
Adesão
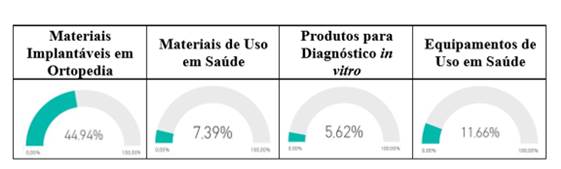
A Agência tem monitorado os percentuais de adesão dos detentores de regularização, por tipo de dispositivo médico. O destaque é para os detentores de registro de materiais implantáveis em ortopedia, que carregaram documentos em 44,94% dos processos de regularização.
Confira abaixo os indicadores para cada um dos tipos de dispositivos médicos:
Confira a íntegra da Resolução da Diretoria Colegiada (RDC) 431/2020.
Acesse também o documento orientativo.
Com informações do portal gov.br (11/12/2020)


